A fémek korróziója és a harc ellene
12. A főbb típusai a fém korróziós
Korrózió - fém megsemmisítés folyamat hatására a kémiai környezet a kapcsolatot vele, zajlik az on-felület felület. Ellentétben fém eróziós korrózió a megsemmisítése a felület hatása alatt mechanikai hatás révén (például, vízsugarak, a hordozó homokszemek, és így tovább. P.).
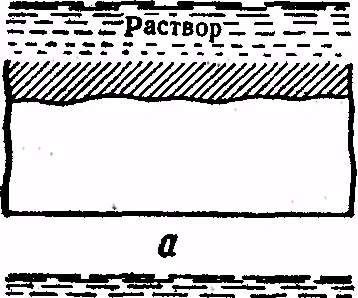
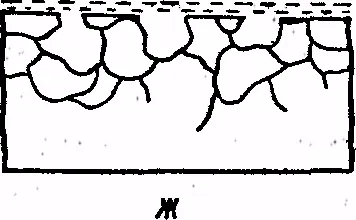
Ábra. 8. A korrózió fajtái:
és - egy egységes, b - blot, egy - g pont - gyümölcsmagozó, d - mezhkristal-litnaya e - repedés, W - Szelektív
A korrózió egy redox heterogén eljárásban határfelületén játszódik. Korrózió léphet fel a gázok, a levegőben, a vízben (folyó, tenger, föld), szerves oldószerekben megoldások és elektrolitikusan-Ing. Megkülönböztetése kémiai és elektrokémiai fémek korrózióját.
A skála a veszteségek a korróziótól rendkívül magas a világgazdaságban. Szó szerint több milliárd dollárt költenek az ipar fejlődése-ügyi országok elleni küzdelem a fémek korrózióját és a csere származik-CIÓ le a fém korrózióját struktúrákat és eszközöket. Így, korróziógátló fém az egyik súlyossága, Ther problémák a termelés és a közlekedésben. korrózió típusok ábrán mutatjuk be. 8. Ez lehet egységes (a); helyi (b - blot, egy - g pont - hámlás); interkristal-litnoy (szemcseközi) (d); repedések (e); szelektív (g).
13. A típusú fém korróziós
Kémiai korrózió - ez a megsemmisítése a fém oxidációs a környezetben előfordulása nélkül az elektromos áram a rendszerben.
Korrózió levegőben különböző hőmérsékleteken. Az intézkedés alapján levegőt vagy valamilyen gáz és fém megváltoztatja állapotát egy felületen, a jellege és mértéke a módosítások meghatározása a tulajdonságait a fém, és a tulajdonságait és összetételét gáz közeg érintkezik a fém. Bizonyos esetekben ez alakult csak egy nagyon vékony réteg a termékek (potuskne-set, sötétedő lágyítás), de gyakran hatása alatt a gáz lép fel erős maró hatású fém (például folyamat rzhavle betétek a vas a nedves levegő) a fém felületén. Az oxidációs a vas van kialakítva a körülményektől függően három oxidréteg tartalmazó FeO, Fe3 O4 és Fe2 O3.
Amikor a fém oxidálódik, a felületén egy réteg oxi-és amelyek, mint a sűrítő, minden egyre több-bonyolítja hozzáférést az oxigén, hogy a fém felületét úgy, hogy a fólia gyakran megvastagodása sebességet nem sebességét kémiai oxidációval a pro-engedményezési és sebességek Tew diffúziója a fémionok vagy oxigén révén a vastagsága a oxidfilm.
Diffúzió útján oxidfilm alapvetően függ a jelenléte hibák. Szobahőmérsékleten, olyan oxidfilm gyakran izo-liruet fém hozzáférést a levegő és az azt követő oxidációja a fém sebesség elhanyagolhatóvá válik. fém oxidáció a levegőn helyezzen nagyobb magasabb hőmérsékleten gyorsan, mivel diffúzió révén az oxidréteget végbe magasabb sebességgel.
Normál nyomáson, fém oxidációja különböző in-hőmérséklet intervallum alá különböző törvények. Például, az alumínium, a száraz levegő gyorsan borított olyan oxidfilm tol-schinoy körülbelül 30 Angström, ami után oxidációt lényegében megszűnik.
A legtöbb matematikai leíró egyenleteket a fémek oxidációját (koordinátákkal rétegvastagság - idő) a szokásos feltételek mellett, logaritmikus vagy exponenciális. Például, ahol - a vastagsága a fólia; K, és - állandók; t - idő az oxidáció. Görbék y = f (t) a 9. ábrán látható (L és C). Felett egy bizonyos parabolikus törvény (F görbe) hőmérséklete megvastagodása oxidfilm hőmérséklet függvényében van kifejezve.
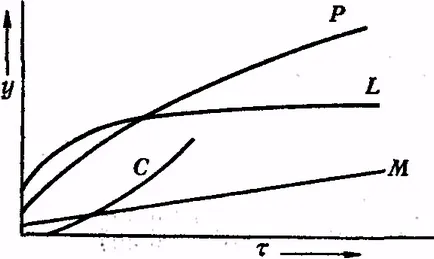
Ábra. 9. Különböző típusú görbék P - parabolikus görbe, L - logaritmikus görbe C - homorú görbe, egy egyenes vonal M
A legegyszerűbb esetben a parabolikus törvény megfelel az egyenlet
ahol - az időt az oxidfilm vastagsága t kezdetétől az oxid-TION, és K és K „- állandók a hőmérséklettől függően, de nem függ az időtől.
Egy kis K értékét (ami igaz a legtöbb szokásos fém-TION a nem túl magas hőmérsékleten), a fém, amely az oxidfilm megvastagszik parabolikus lehet tekinteni a szakterületen, hogy kellően ellenáll az oxidációnak, olyan oxidfilm, ha ez nem egy raszter-skivaetsya. Magasabb TEM-középhõmérséklete, különösen egy olyan atmoszférában, amely kis mennyiségű savanyú jellegű, vagy csak gyenge oxidálószerek, oxidációt gyakran együtt jár egy közel állandó-sósav sebesség. Ez lehet egy szélsőséges esetben, ha az oxidációs sebessége független az időtől, akkor a fólia vastagsága lehet alábbi egyenlet fejezi ki neniem-növekedés oxidfilmeket a fém kristályok y = Kτ + K` (line M a grafikon)
Gyakorlatilag nagyon fontos pro-folyamat vas korróziós légköri viszonyok közönséges tempera-fordulók (rozsda). Rozsdásodó vasat nagyon gyorsan nedves levegő. Meg kell jegyezni, hogy a folyamat megy vas rozsda maximális intenzitással páratartalom, ami nem reagál teljesen telíti a levegő vízgőz. Ha a relatív páratartalom 65% korróziós sebességet viszonylag-nagy, és a 65% feletti ez nagyon gyorsan növekszik, azonban, a relatív páratartalom 65% -os sósavval úgynevezett kritikus relatív páratartalom mellett. Ha a kritikus és a magasabb páratartalom rozsda, amely higroszkópos, erősen vonzza és megtartja a nedvességet. Kezdetben narancssárga rozsda egy gélszerkezet, de fokozatosan a kristályos oxid
-hidroxid (FeO) OH. Kristályosítás indul belső réteg rozsdás-soraiban, ahol a külső héj a gél, amely nagyon törékeny, lebontja a száraz állapotban. A végtermékek a folyamat rzhavle-TION vannak a- és y-módosítási FeO (OH) és a Fe3 04.
A fémek oxidációját a levegő fokozott a szennyeződések jelenléte a kén-dioxid, szén-dioxid, halogének, savak, és a vízgőz. Így alakul ki a felületén a fém-szulfát (szulfitok vagy szulfidok), karbonátok és esetleg hidroxidok, CO-torye gyorsan elbomlanak, ami a másodlagos oxidok több porózus és kevésbé védi a fémet a korróziótól. Során a fém korrózióját fontos szerepet játszik a kapcsolatot más fémekkel vagy akár szilárd anyagokat, mint például a por jelenlétének a fém felületén. A poros levegő korrózió jelentős-de intenzívebb, mint a tiszta por.
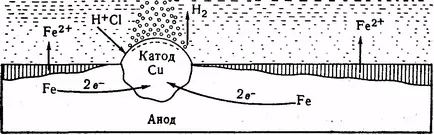
Ábra. 10. Az áramkör a felvétel a vas korróziós réz
Galvanikus korrózió. A pusztítás fém egy közepes elektro-Lits eseménynek a villamosenergia-rendszer az úgynevezett elektrokémiai korrózió. Gyakorlatilag bármilyen fém, amely szennyezést tartalmaz egyéb fémek. Ezért, egy elektrolit közegben rendszert az alapfém és a fém szennyező P képez számos mikro-galvánelemek. Előfordulása az ilyen elemek lehet magyarázni; Ob-alapú értékei standardpotenciál (táblázat. 3.). Minden tag ebben a sorozatban, fölött álló egy nagyobb negatív potenciál, mint a szomszéd alább. Természetesen, ha a két fém vezetővel, hogy csatlakoztassa a megoldást, és oldatba helyezzük ionokat tartalmazó őket, az aktívabb a fém korrodálják, míg a kevésbé aktív korrózió nem egy al-elutasítják.
Ábra. A 10. ábra a lemez a vas réz zárványok. Az elektrolit-oldatot (HCI), ez a rendszer egy horganyzott-nikai elem, amely a vas Ano-ház a belső láncot (E ° = - 0,44 in), és réz - katód (E ° = 0337 a). Atomjai vas, réz átvitele két elektront átadni oldatba formájában Fe 2+ ionok a közepes és klorid-ionok vas-klorid (II). A hidrogén ionok mozognak, hogy a katód (réz). Itt helyezze zhayutsya:
A kapott hidrogén-részben megtartja katód felületét részlegesen eltávolítjuk a buborékok formájában. Ha nem adják át a katód az oxigén, majd fokozatosan kezdődik annak polarizációját. katód potenciál válik negatív, és végül képest potenciálok az anód, amely megszűnését okozza a jelenlegi és a korrózió. A SLE-tea mentes levegő oxigén a katód bekövetkezik Depot polarizációja
és elektrokémiai korróziós folyamat megy simán. Ha ez a galvanikus elem helyett sósavat, hogy az oldat nátrium-klorid, általában az eljárás során nem változtatta volna. Elfogadja lenne, ha csak másodlagos reakciókat. A katód, továbbá a hidrogén, nátrium-hidroxid keletkezik: