A szerkezet a vízmolekulák - Hydrogeology
Víz - az egyik leginkább figyelemre méltó anyag ismert ember. Ő - az egyetlen természetes anyag található nagy mennyiségben a három állam: szilárd, folyékony és gáznemű. Az összes szokásos folyékony víz - legsokoldalúbb folyékony oldószer maximális értékei a felületi feszültség, dielektromos állandó, és a magas hő párologtatás (miután ammónia) fúziós hője. Ellentétben sok anyag, víz, fagyasztás alacsony nyomáson tágul.
Ezek a különleges tulajdonságok a víz kapcsolódnak a speciális szerkezete a molekulái. Kémiai képlet H2 0 vízzel megtévesztően egyszerű. A vízmolekula hidrogénatomok a sejtmagban vannak elrendezve képest aszimmetrikusan a magja egy oxigénatom és elektronok. Ha az oxigén atom közepén egy tetraéder, a tömege központok két hidrogénatom van a sarkokban egy tetraéder, és feltölti a központok két elektron pár elfoglalni két másik sarokban (ábra. 3.1). Így, négy elektron vannak elrendezve a lehető legnagyobb távolság mind az oxigénatom a mag, és a sejtmag a hidrogénatomok amelyekhez húzott mag oxigénatom. Egyéb hat vízmolekulák elektronokat úgy vannak elrendezve, négy elektron abban a helyzetben, hogy egy kémiai kötés között a magok az oxigén és hidrogén atomok és a másik kettő található, közel a nucleus oxigénatom.
Az aszimmetrikus elrendezése az atomok a víz molekula okozza egyenetlen Az elektromos töltések eloszlása abban, hogy a poláris vízmolekula. Egy ilyen szerkezet a vízmolekula okoz a vízmolekulák vonzódnak egymáshoz eredményeként a hidrogén kötések kialakulását közöttük. Hely hidrogén és oxigén atomok vízmolekulák kialakult aggregátumokat hasonló az elrendezése a szilícium és oxigén atomok a kvarc. Ez vonatkozik a jég, és a legalább egy folyékony víz molekulaagregátumoknak amelyek mindig újraelosztásával lépésben. Lehűtéskor vízmolekulák vannak csoportosítva aggregátumai, amelyek fokozatosan nőtt, és egyre ellenálló ahogy közeledik a hőmérséklet 4 ° C-on, amikor a víz eléri a maximális sűrűsége. Ezen a hőmérsékleten, a víz még mindig van egy merev szerkezet, és ezzel együtt a hosszú láncú molekulák, van egy nagy számú egyedi vízmolekulák. A további hűtővíz molekulaláncok növekedni Hozzáadunk szabad molekulák, ahol a víz sűrűsége csökken. Amikor a víz átalakul jég, minden molekulák többé vagy kevésbé merev szerkezet formájában nem zárt láncok alkotó kristályok.
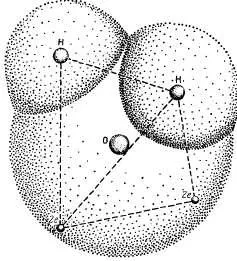
Ábra. 3.1. A szerkezet a vízmolekula.
A kölcsönös penetráció a hidrogén és oxigén atomok. A magok két hidrogénatom, és két pár elektronok a sarkokban egy tetraéder: központban a mag oxigénatom.
Nagy értékű felületi feszültség és hő párologtatás vizet annak a ténynek köszönhető, hogy a víz molekulákat elválasztjuk a csoport molekulák igényel egy viszonylag nagy energiaráfordítás. A vágy a vízmolekulák a hidrogénkötést létesítsen és polaritás magyarázza a szokatlanul nagy vízoldhatóságú. Egyes vegyületek, mint például a cukrok és alkoholok, megmaradnak az oldatban miatt hidrogénkötések. A vegyületek, amelyek a magas fokú ionizációs a bemeneti, mint például a nátrium-klorid, megmaradnak az oldatban annak a ténynek köszönhető, hogy az ionok semlegesítjük ellentétesen töltött csoportok orientált vízmolekulák.
Relatív előfordulását és felezési a hidrogén izotópjai és oxigén