alkánok előadás
Fizikai tulajdonságai alkánok - lásd a bemutató ..
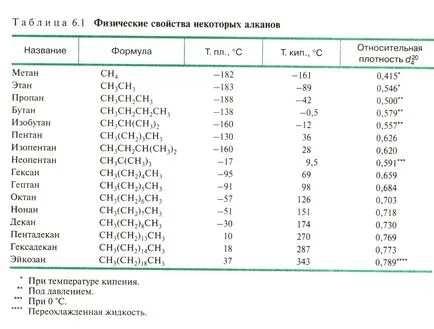
Előállítására szolgáló eljárások alkánok
Forrásai az ipari termelés alkánok - földgáz, olaj.
Szintetikus módszerek (elsősorban a laboratóriumban hogy komplex alkánok):
1. A hidrogénezést az alkének és alkinek
2. helyreállítása halogénezett alkánok
4. Wurtz reakció
5. Kolbe Reakció
Vegyi reakció - ez általában többlépcsős folyamat. Kezdődik, a törés a kötések a kiindulási vegyületek, majd a kialakulását új kapcsolatok és új kapcsolatokat. A reakció során, instabil köztitermékek részecske. A lépések sorrendje a reakció mechanizmus nevezik.
Az aktív részecske - részecske, amelynek nagy kémiai aktivitást, akkor a reakció megindításához.
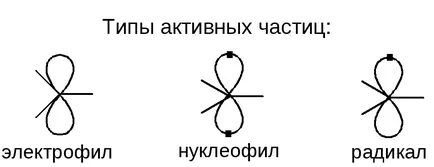
Elektrofil - elektron-részecske támadások fokozott elektronsűrűség helyet.
Nukleofil - ELECTRON részecske támadások helyeken csökkentett elektronsűrűség.
Radical - elektromosan semleges részecske, támadó nem poláros, enyhén poláros kötés.
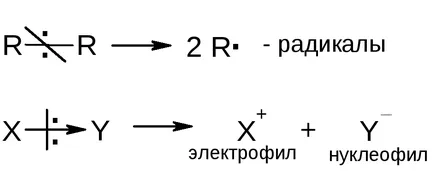
Az aktív részecskék képezhetők megtöri a kémiai kötés. Homolytically kevéssé poláros kötések megszakadnak, és két gyökök keletkeznek; poláris kötések bomlanak heterolytically és formázott nukleofil és elektrofil:
Kémiai tulajdonságait alkánok
Alkánok - a legtöbb kémiailag inert anyag.
C-C kötés és C-H alacsony polaritású, és ellenálló a támadás elektrofil és nukleofil, törnek hatására gyökök.
reakció mechanizmusa - lánc-csoport:
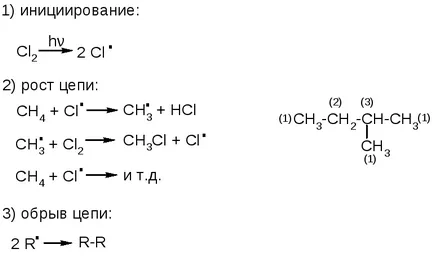
A reakció sebessége a primer, szekunder és tercier szénatom eltérő: növeli a sorrendben: C (1) <С(2) <С(3) (см. предыдущую схему).
Továbbá klórozás kicsit szelektív ebben a tekintetben, sokkal szelektívebb brómozásával kisebb Br-aktivitás.
a gőzfázisban 400-500 °;
folyékony fázis - körülbelül 110-140 (Konovalov)
Alkánok - az egyik legnehezebb oxidált anyagokat. Szobahőmérsékleten még csak nem is az erős oxidálószerekkel.
A belső égésű alkánok konvertálódnak CO2 és H2 O.
Szabályozott oxidációját oxigén körülbelül 200 és 90 atm. bevételt a folyadékfázisban a hasítási C-C kötést, míg a kialakulását keverékéből karbonsavak.
Például, ipari eljárás előállítására ecetsav:
3. Thermal felosztása és repedések:
Repedés igen széles körben használják a kőolaj finomítás a magas oktánszámú üzemanyagot.
Egyes képviselői alkánok - lásd a bemutató ..
Cikloalkánok - telített szénhidrogének egy zárt áramkört.
Az általános képlet - CnH2n (monociklusos szubsztituálatlan).
Ezek különböznek cikloalkánokból:
- Eljárás összekötő ciklus.
Monociklusos. a ciklopropán, ciklobután, ciklopentán, ciklohexán
(Forma magyarázó).
a) a kondenzált (anellált):
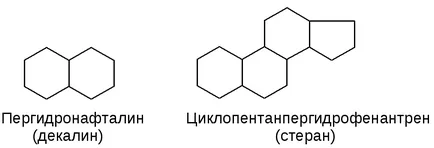


Elmélet feszültségek (Bayer)
Az eltérés a geometriai szög a kötés szöge 109 feszültséget állít elő a ciklusban:
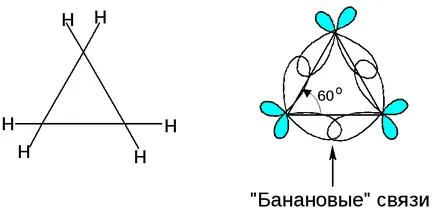
„Banán” kommunikációs közbenső jellegű közötti π- és σ-kötések: telítetlen ciklopropán - Kapcsolási reakció ciklust egy szünetet.
Előállítására szolgáló eljárások cikloalkánok
1. dehidrogénezés dihalogén-alkán (variáns Wurtz reakció):
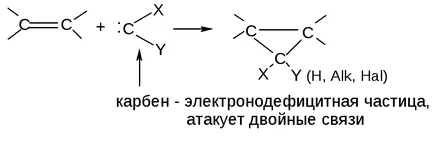
3. A dién-szintézis (Diels-Alder-reakció):
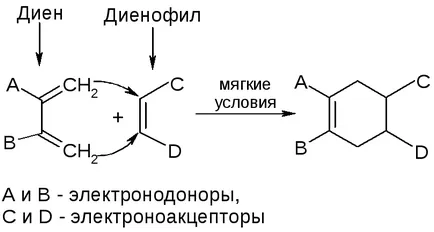
A kémiai tulajdonságai cikloalkánok
1. Reakciók kis ciklusok:
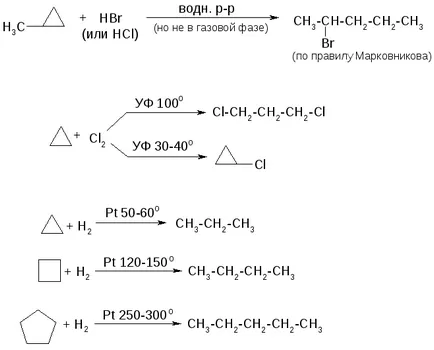
2. reakciók másodlagos ciklusok majdnem ugyanaz, mint a gyűrűs alkánok.
Egyes képviselői a cyclo - lásd a bemutató ..