Benzol - kémiai enciklopédia
A benzolos molekula - egy lapos szabályos hatszög ext. szögek 120 °, és a távolság között a szénatomok között 0,139 nm. Az UV-spektrum etanolban maximuma 184 nm-nél (lg 4,77), 203,5 nm (lg 3,87), 254,5 nm (lg 2,31).
Benzol - az őse aromás szénhidrogének. sorozat. Chem. Holy Island jelenléte határozza meg a molekulában stabil elektron zárt rendszer (lásd. Aromásságának. Aromás vegyületek). Ő hajlik a donor-akceptor kölcsönhatás. csatlakozó. amelynek hiányossága elektronok; kialakulását eredményezi gyengén stabil, és már csak a p-rahkompleksy, to- alakítjuk. További prochnyekompleksy. Benzol képes komplex képződését határozza meg a tendencia, hogy elektrofil. -naib csere. jellemző a p-benzolt tsiyam pl.
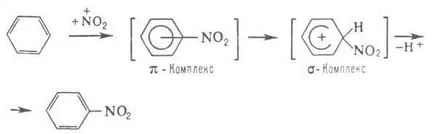
Katalizátorok elektrofil. csere - általában akkor, Lewis, kialakulását elősegíti a közbenső. komplexek és felgyorsítja az ömlesztett p-TION, például. klórozás.
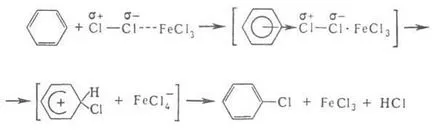
A benzolt szulfonálhatunk, benzolszulfonsav. alkilezzük olefin alkotnak LAB. Attól függően, hogy a szubsztituens természetétől további először elektrofil. preim irányított helyettesítés. orto- és para-helyzetben, vagy a meta-helyzetben.
Benzol jellemző a nagy ellenállás a T-P és oxidáló szerekkel. Csak a fenti 650 ° C-on az részben alakítjuk. difenil. felett 750 ° C-on bomlik szénre és hidrogénre. Benzol nem változik hatására H2 SrO4 és KMnO4. O2 jelenlétében. katalizátorok (V, Mo) 350 ^ 450 ° C-on a maleinsavanhidrid formák. Hidrogénezzük, hogy ciklohexán jelenlétében. december katalizátorok (pl. jelenlétében. Ni át 120-200 ° C-on és 2,96-6,94 MPa). Alkálifémek folyékony NH3 redukáljuk 1,4-ciklohexadiént. Amikor fotokémiai. Csatlakozási klórt alakítjuk. A hexaklór. Amikor az UV besugárzás képes cikloaddíciós és izomerizációt fűlvén (I) általános képletű és benzvalen (II).
Naib. A régi módszer a bálba. termelő benzol: izolálás annak előre lehűtött pirogazovyh termékek Kokszolható szenek abszorpciós Org. mosogatók, pl. olajok kam.-ug. és kőolaj eredetű; abszorber elválasztására vízgőzdesztillációval. Szennyeződéseket (pl. Tiofén) nyers benzol elválasztva, amelyet hidrogénezés. DOS. Mennyiség benzolt kapott reformáló (470-550 ° C) ásványolaj frakció forraljuk 62-85 ° C-on; extrakcióval kinyerjük. Benzol nagy tisztaságú kapjuk extrakciós desztillációval DMF. Benzol szintén elválasztjuk a folyékony termékek pirolízis olajat. alakult etilén és propilén termelés-ve. A feleslegben toluol dezalkilezési előállítására benzol források utolsó-Roe szokásos termikus végre. módszer 600-820 ° C jelenlétében H2 és gőz, vagy katalitikusan át 227-627 ° C-on jelenlétében. zeolitok, illetve -oxid katalizátorral. Naib. gazdaságilag legelőnyösebb kiválasztási benzol pirolízistermékek. de a források ezt a forrást nem elegendő, így io Ez által termelt reformja. A részesedése kólát. benzol teljes egyenleg kicsi. A laboratóriumokban nagy tisztaságú benzol előállítása dekarboxilezésé benzoesav a-te.
Sajátosságai. p-CIÓ detektálás jelenlétében benzol. homológok: szénhidrogén-keveréket összerázzuk ammóniával p-rum Ni (CN) 2; benzol jelenlétében kicsapódik komplex comp. Ni (CN) 2 NH3 (C6 H6).
T benzolra. Aux. - 11 ° C, t ÖNGYULLADÁSI .. 534 ° C-on, 1,5-8% CPV. Ez irritálja a bőrt; benzol nagy koncentrációban van egy görcsös fellépés; ismételt expozíció alacsony koncentrációban, változások figyelhetők meg a vérben és a vérképző szervek; MPC 5 mg / m 3.
Szállítják a vasúti tartálykocsik, felszerelése az ételek melegítéséhez. Benzol fedezte fel Michael Faraday 1825-ben a pirolízis a bálna olaj; E. Mitscherlich először szintetizált 1833-ban dekarboxilálására benzoesav, hogy Te.
===
App. Irodalom A cikk „A BENZOL”. Sokolov 3. Kharlampovich GD gyártását és használatát az aromás szénhidrogének. M. 1980; Efross Gorelik L. S. M. Chemistry and Technology intermedierek, L. 1980 Összes szerves kémiában. per. az angol. Vol. 1, M. 1981, p. 314-455. NN Artamonov.