Meghatározása elektród potenciál fémek
fizika és a technológia az optikai kommunikáció
Laboratóriumi munka №5
MEGHATÁROZÁSA FÉMEK elektród potenciál
Határozza meg az elektróda potenciál Cu, Pb, Zn, Fe, Ni. Ahhoz, hogy tanulmányozza a változását elektród potenciálját a cink, attól függően, hogy a koncentráció a cink-só oldathoz.
Bármely fém oldhatósága az elektrolitban, bár jelentéktelen. Ha a fémlemez merítjük, például, a víz, a fémionok eredményeként ezek poláros vízmolekulák lecsúszhat a felületről, és bemegy a szomszédos réteg a víz; úgy, hogy mielőtt semleges atom alakítjuk, egy pozitív töltésű ion:
A folyamat dinamikus jellegű, úgy, hogy az elektrolitban a fém felületén, hogy hozzon létre egy újraelosztása koncentrációjú oldószer és fém ionok és oldószer molekulák.
Így, interakció a fém vízzel vagy egy oldatot tartalmazó ionokat a fém, így a formáció a felületén elektromos kettős réteg, és a megjelenése között potenciálkülönbség a fém és az oldatot. Ez a potenciális különbség tartalmaz egy potenciális csepp a réteg adszorbeált felületi ionok (JA), valamint a feszültségesés az oldatban (a diffúziós réteg (Jd):
Átmenetifém-ionok oldatban - egy reverzibilis folyamat és izotermikus, itt a rendszer a lehető legnagyobb hasznos munkát A. jellemezve izobár-izoterm potenciális Gibbs DG ° p:
ahol n - az ion töltése; j - a potenciális különbség a fém és az oldatot, F - Faraday számát.
Egyensúly dinamikus: a felületi réteg részét -ionok diffundálnak az elektrolit, más ionok az oldatból helyettesíti őket. Ennek eredményeként, az egyensúlyi koncentrációja a fémionok az elektród felületén a C0 is más, mint az átlagos koncentrációja az ionokra oldatban C.
Izotermikus művelet mozgó ionok közötti 1 mol, és az összeget a felületi réteg az oldat úgy definiáljuk, mint:
A feltétel, hogy ezek a művek kell:
Innen megtalálható az elektród potenciál:
C0 koncentráció kísérletileg határozzuk meg lehet, így a lehetséges az izolált elektród elmerül az elektrolit oldatban, ez nem lehet számítani. Azonban, meg lehet határozni a különbség a potenciális (EMF = DE = J2 - J1) közötti azonos merített elektródák előállítása saját ionok, de különböző koncentrációjú, úgynevezett koncentráció cella:
vagy standard körülmények között (298 K), és cseréje után a természetes logaritmusa decimális:
A elektrokémia A elektróda fém általában mérni potenciálok voltban, kijelölt E, viszonyítva a standard referencia elektród, amely a potenciális hagyományosan venni nulla. A nemzetközi megállapodás, mint például egy referencia elektród, a standard hidrogén elektród használunk. fiktív mennyiség jellemző a lehetséges az elektród vizsgált, szedi az EMF a sejt, tagjai ennek elektróda és egy standard hidrogén elektród. Ez a mennyiség az úgynevezett elektród potenciálja az elektróda és a jelöli a betű o. Így, figyelembe a fémionok koncentrációját a adszorbeált réteg C0 = 1 mol / l, megkapjuk EMF eleme egy típusú fém, de különböző koncentrációjú ionok oldatban:
ahol CMe n + - moláris koncentrációja ionok.
Ez az egyenlet az úgynevezett Nernst-egyenlet.
Az egyenlet közelítő, mivel nem veszi figyelembe ion-ion kölcsönhatás elektrolit oldatok. injektált ion aktivitás társított koncentrációját következő egyenlet fiókot e kölcsönhatás:
ahol f - aktivitási együttható.
Az egyenlet kiszámításához elektródpotenciál is a formája:
Az, hogy a teljesítmény
Végzett munka két szakaszban: az első szakaszban mérjük standardpotenciál fémek, amikor elmerül megoldásokat a megfelelő sók koncentrációja 1 mol / l; egy második lépésben a függőség a elektród potenciálját a fém (cink) merítve egy cink-sót különböző koncentrációjú vizes oldatainak: 0,1 M; 0,5; 1,0 és 1,5.
1. Kap egy sor elektródákat.
2. mérések előtt minden egyes alkalommal, hogy a szalag csiszolópapír felületi elektródával.
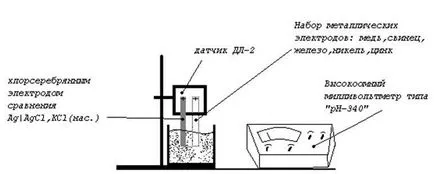
3. Egymást követően vizsgáltuk kapcsolt elektródák vannak az érzékelő, ami az áramkör a galván mérőelektród és ezüst-klorid referencia elektród. Mindkét elektródák így kell szállítani, egy alkalmas só oldatát a kívánt koncentrációra.
4. Az eszköz határozza meg az EMF.
5. Számítsuk értékét a mért feszültség (DE) mV. Erre a célra az olvasó egység kapott szorozva 100.
6. Minden egyes mérés után az ezüst-klorid elektródát kell desztillált vízbe merítjük.
Elvégzett kísérletek és a szükséges számításokat, meghatároztuk az elektród potenciál a réz, ólom, vas és nikkel, valamint vizsgáltuk a változását az elektród cink kapacitás koncentrációjától függően a cinksó-oldat és a hiba volt, 15% -ról 24% miatt hibás tisztítási elektród minden mérés előtt.
Szintén találtunk néhány különbség elmélet és gyakorlat:
A növekvő koncentrációjú cink megnövelt elektród potenciálja
Kapcsolódó elemek
Információ a munkát
Jelentések a laboratóriumi munka
A fájl kinyomtatásához, töltse le (Word formátumban).