Szabályozók alternatív poliadenilációs mRNS
„Molekuláris gép” vagy tényezők, és enzimek
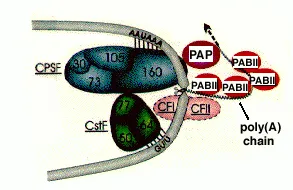
A vágási igényel hasítási / poliadenilációs faktor I (CPSF) (vágás faktor / poliadenilációs) és a hasítási faktor II (CF II), mint betöltéséhez szükséges-poli (A) polimeráz (poli (A) polimeráz (PAP1)), hasítási faktor I (CF I), poliadenilációs faktor I (PF I) és Pab1 vagy NAB2 (lásd. ábra). CF II, PAP1, és PF I izolálhatjuk, mint egy nagy és összetett a CPF. Az összes gén részt ebben a folyamatban azonosították kombinációja biokémiai és genetikai módszerekkel.
mozgás:
Multiprotein komplex biztosít vágás pre-mRNS 15-30 nukleotid helyben elismert CPSF. Leggyakrabban, az oldal tartalmaz AAUAAA-szekvenciát, de lehetnek más lehetőségek, de a kötődés CPSF gyengébb. CstF (hasítás stimuláció faktor, faktor stimuláció vágás) kötődik c GU-gazdag régió a helyszínen. A harmadik felismerési hely tartalmazó UGUAA-szekvenciát kötődik a CFI, ami aktiválja CPSF akkor is, ha ez nem jár együtt AAUAAA. RNS vágják után azonnal a transzkripciós egyszer CstF kötődik az RNS-polimeráz II. Ezen túlmenően, a vágórész CFII, de a részletek még nem ismertek.
Amikor kész vágás, poliadenilációs elkezdi használni a PAP. Ez növeli a 3'-végén az RNS AMP (adenozin-monofoszfát) az ATP. hasító pirofoszfát. PAB2 társított új, rövid poli (A) farok és PAP növeli affinitása az RNS-t. Amikor a farok eléri a hossza körülbelül 250 nukleotid, így az enzim elveszti kommunikáció CPSF és poliadenilációs leáll. CPSF érintkezve RNS polimeráz II és a transzkripció leáll. Ezen túlmenően, egy multiprotein komplex svyazyvaetsyacherez CFI azzal spliceosome, amely eltávolítja az intronok RNS-ből.
Ez a rendszer leírható még:
Egy kicsit közelebbi pillantást a PAP, amely a professzor szavaival Claire Moore a Boston Tufts Egyetem, egyfajta „szíve” E molekuláris gép. Tanulmányok Claire Moore és Andrew Bohm azt mutatta, hogy a PAP áll 3 domének 150-200 aminosavak egyes. N-terminális domén-családba tartozik, a transzferázok és nukleotidok tartalmaz egy hármas jellemző aminosav. Ezek az aminosavak részt vesznek fém-kötő szabályozott foszfátcsoport az ATP, és képes a elhelyezése a nukleofil 3'-OH (hidroxi) primer, ami megkönnyíti a katalizált reakció nukleotid-transzferáz.
Az átlagos tartomány PAP nem rendelkezik szerkezeti homológiát mutat a más fehérjékkel. Tanulmányok kimutatták, hogy részt vesz a kölcsönhatás a foszfátcsoport az ATP és pirofoszfát eltávolítjuk, valamint az az RNS transzlokációja a következő szakaszában poliadenilációs.
C-terminális domén szükséges retenciós poli (A) - a primer a helyén.

A választás a poliadenilációs hely fordul függően fehérjék vesznek részt. Például, expressziója CstF-64 alegységet CstF, növeli a makrofágokban válaszul lipopoliszacharid (a komponens a bakteriális fal, amely beindítja az immunválaszt). Ez a választás eredménye gyenge poli (A) -hely-szintézis és ennek megfelelően rövid transzkriptumok megszüntetése szabályozó elemek a 3'-végi nem transzlálódó régiót az mRNS, mint védelmi összetevők, mint a lizozim és a TNF-α. Ezek mRNS nagyobb a várható élettartam.
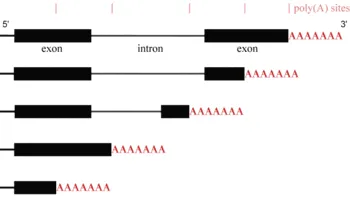
Alternatív poliadenilációs ugyanazon gén szövet-specifikus jellegét, sőt, ez változó élettartama során a sejt. A kutatások szerint a tudósok a University of Medicine és fogorvosi New Jersey azonosítani lehet a 42 különböző típusú alternatív poliadenilációs. Azt találtuk, hogy bizonyos szövetekben használt poliadenilezési helyek, amelyek egy bizonyos helyen, a gén, például lokalizált oldalak belül intronok vagy exont és nagy belső helyek exon lokalizált közel a 3'-végén. Szintén szöveti detektáltuk (a szem szöveteit, retina, méhlepény), amelyek használata oldalak ritkán használják más szövetekben. Ez analizáltuk körülbelül 20 gének, amelyek fehérje termékek vesznek részt a szabályozásában poliadenilációs. Néhány agyszövet bizonyítani magas szintű megfelelés ezen gének expressziója, de az alacsony szintű összhangot más szövetekben. Ha összehasonlítjuk a genomiális régiók körülvevő a poli (A) -sites, főleg az agyban szövetekben, azzal területek a más szövetekben azonosítottak néhány cisz-szabályozó szekvenciák specifikusan kapcsolódó poli (A) -hely használja az agyban szövetekben.
Alternatív poliadenilirovanie- egy összetett folyamat, amelyek szabályozása még nem teljesen világos. Most sok laboratóriumok foglalkozik a kutatás alternatív poliadenilációs mRNS szintetizált különböző génekből, például NO-szintáz (enzim-szintézis-oxid azota- anyag szintetizált hajók és okoz azok kiterjesztésére), ciklooxigenáz (kulcsenzim a metabolizmusát arachidonsav ksiloty amellyel szintetizált gyulladásos mediátorok) és még sokan mások.
Ezek a vizsgálatok neobhodmy, de emellett van szükség:
1), hogy vizsgálja meg a szabályozó szekvenciák
2), hogy vizsgálja tényezőből poliadenilezési
3) szervezni tanulmány poliadenilációs a mRNS szintetizált különféle gének